|
|
1 Definirea notiunii de radical liber
Exista mai multe definitii ale termenului de radical liber dar cea mai simpla definitie adoptata de Halliwel (271) este urmatoarea: radical liber este orice specie capabila de o existenta independenta care contine unul sau mai multi electroni nepereche. Un electron nepereche este acel electron care ocupa singur un orbital atomic. Prezenta unuia sau mai multor electroni nepereche determina atractia cu usurinta a radicalului liber catre un camp magnetic si ii confera acestuia o inalta reactivitate.
Radicalii pot fi formati cand o legatura covalenta se rupe si fiecare electron ramane la cate unul din atomi, proces numit fisiune homolitica.(272) Energia necesara pentru ruperea legaturii covalente poate fi obtinuta prin incalzire, radiatie electromagnetica etc. Foarte multe legaturi covalente se rup la temperaturi inalte (450 -600˚C), in special legaturile carbon-carbon, carbon-hidrogen, carbon-oxigen. Combustia este binecunoscuta de chimisti ca un proces producator de radicali liberi.
Daca A si B sunt 2 atomi legati printr-o legatura covalenta, fisiunea homolitica poate fi scrisa astfel:
![]() A:B A + B
A:B A + B
De exemplu, fisiunea homolitica a unei legaturi covalente O-H din molecula de apa, genereaza radical hidrogen- H si radical hidroxil OH.
4.2 Speciile reactive ale oxigenului
Termenul de specii reactive ale oxigenului(ROS) este folosit larg pentru a cuprinde atat radicalii liberi ai oxigenului cat si speciile non radical ( TABEL 1)
Una din cele mai populare teorii care explica toxicitatea oxigenului este teoria toxicitatii radicalului superoxid (O2) specie reactiva derivata din oxigen a carui supraproductie determina efecte nocive asupra tesuturilor.
TABEL 1
o Speciile reactive ale oxigenului:
Radicaliliberi::
- Radical hidroxil: HO*
- Radical superoxid: O2-
Neradicali:
- Peroxidul de hidrogen: H2O2
- Oxigenul singlet: 1O2
o Produsi ai peroxidarii lipidelor:
- Radical peroxil: ROO*
- Radical al koxil: RO*
o Produsi secundari:
- Malondialdehida
- 4-hidroxialkenali
dupa Conklin KA.(273)
Superoxidul este produs in mod fiziologic, de exemplu in celulele fagocitare. Unele enzime, cum e xantin-oxidaza, au capacitatea de a reduce O2 la O2, proces catalizat de xantin-dehidrogenaza. Radicalul superoxid este produs si prin oxidarea unor molecule ca: gliceraldehida, FADH2, hormoni (adrenalina, noradrenalina, dopamina) sau prin oxidarea fierului din hem cu formare de methemoglobina.
Cea mai importanta sursa de superoxid in vivo, in celulele organismelor aerobe, este lantul de reactii transportoare de electroni din mitocondrii. In conditii fiziologice 1-3% din O2 este redus la O2. (274)
Productia de radicali ai oxigenului prin respiratia mitocondriala poate contribui la lezarea proteinelor, lipidelor si ale ADN mitocondrial, leziuni ce se accentueaza cu varsta.(275,276)
In afara de speciile reactive ale oxigenului, organismele vii produc o gama larga de radicali liberi.(Tabel 2).
Exemple de formare a radicalilor liberi sunt numeroase: proteinele ce contin gruparea thiol (R-SH) oxideaza in prezenta ionilor metalelor tranzitionale, rezultand radicali tiil.(RS)
![]() R-SH + Cu2+ R-S
+ RS + Cu+ + H+
R-SH + Cu2+ R-S
+ RS + Cu+ + H+
Tabel 2. Exemple de radicali liberi (271)
|
Nume |
Formula |
Observatin |
|
Atomul de hidrogen |
H |
Cel mai simplu radical liber |
|
Triclormetil |
CCl3 |
Radical al carbonului, produs in ficat din CCl4 contribuie la efectele toxice ale solventului. Radicalii carbonului reactioneaza rapid cu O2 formand radicali peroxil |
|
Superoxid |
O2 |
Radical al oxigenului |
|
Hidroxil |
OH |
Radical al oxigenului cu reactivitate crescuta, ataca toate biomoleculele |
|
Til/pertil |
RS/ RSS |
Grup de radicali care au electron nepereche la atomul de sulf. |
|
Peroxil, alcoxil |
RO2, RO |
Radicali ai oxigenului formati prin descompunerea peroxizilor organici si reactia radicalilor carbonului cu O2 |
|
Oxizi de azot |
NO, NO2 |
Oxidul nitric se formeaza in vivo din amino acidul L-arginina.Dioxidul de azot rezulta din reactia NO cu O2 Ambii se gasesc in aer poluat, fumul de tigare |
|
Radicali ai azotului |
C6H5N= N |
Se formeaza prin oxidarea fenilhidrazinei in eritocit |
|
Ioni ai metalelor tranzitionale |
Fe, Cu |
Abilitatea de a-si schimba pe rand gradul de oxidare, le permite fie sa accepte fie sa doneze electroni; de aici puterea lor de a cataliza reactiile radicalilor liberi. |
Peroxidarea lipidelor genereaza radicali liberi ai carbonului.
Unii oxizi ai azotului NO si NO2 sunt radicali liberi, ceea ce a condus la introducerea unui nou termen, cel de specii reactive ale azotului(RNS).
2.Surse de formare a metabolitilor oxigenului
Interesul comunitatii stiintifice de specialitate pentru reactiile in care apar specii reactive ale oxigenului (SRO) este sustinut nu numai de numarul mare de procese in care apar ci si de diversitatea absolut surprinzatoare a acestora (277). SRO se formeaza constant in celule in diferite procese metabolice, sursele de formare fiind fie endogene, fie exogene (278).
Tabel 3. Surse de formare a metabolitilor oxigenului
Surse endogene - lantul de transport de electroni din mitocondrii,
- activitate enzimatica (oxidaze,ciclooxigenaze, lipoxigenaze)
- activitatea leucocitelor polimorfonucleare, macrofage
- oxidarea hemoglobinei, catecolaminelor, tiolilor
Surse exogene - metabolizarea unor xenobiotice, medicamente, aditivi alimentari
- iradieri cu UV, radiatii ionizante,
- metabolizarea unor poluanti chimici (nitriti, solventi, barbiturice, gaze iritante , derivati de azot, sulf, etc.)
Radicalii liberi intermediari ai reactiilor enzimatice scapa din centrul activ ca urmare a unor interactiuni accidentale cu O2 sau alti compusi. H 2O2 astfel format este eliberat in mediu si va genera HO . (279). Medicamentele, radiatiile UV, aerul poluat, agenti chimici pot induce supraproductia de SRO in celule (280). Astfel, spre exemplu, neuronii dopaminergici, implicati in boala Parkinson, sunt susceptibili la efectul citotoxic al SRO. Prin degradarea dopaminei rezulta H 2O2 care genereaza HO . prin reactii Fenton (281).
Tetraclorura de carbon (utilizata frecvent ca solvent in curatatoriile chimice) este convertita intr-un radical liber extreme de reactiv care poate fi implicat in geneza necrozei hepatocelulare(282).
Doxorubicina induce afectiuni cardiace prin stresul oxidativ generat in mitocondriile miocardului. Acest medicament interactioneaza cu lantul respirator in punctul dintre coenzima Q si oxigen, generand radicali hidroxili toxici (283).
2. Modul de actiune al radicalilor liberi
Reactivitatrea radicalilor liberi depinde de tipul de radical si cu cine intra in reactie.
Astfel, daca doi radicali liberi intra in contact, ei isi unesc electronii nepereche intr-o legatura covalenta:
![]() H + H H2
H + H H2
Un exemplu mult mai relevant biologic este reactia foarte rapida dintre radicalul oxidului nitric (NO) si radicalul superoxid, cu formarea unui non-radical, peroxinitrit. (284).
![]() NO + O2 ONOO
peroxinitrit (non-radical)
NO + O2 ONOO
peroxinitrit (non-radical)
Daca radicalul liber reactioneaza cu un non-radical, se formeaza un nou radical, si lantul de reactii continua. Ex. radicalul hidroxil (OH) reactioneaza cu guanina din ADN si rezulta un nou radical 8-OH-guanina.
Un radical poate fi agent reducator, donand electronul nepereche unui non radical, care devine astfel radical. Ex. reducerea ionului de cupru (Cu+) care acceptand un electron devine radical Cu .
![]() CO2 + Cu+ CO2 + Cu
CO2 + Cu+ CO2 + Cu
Un radical poate fi agent oxidant, acceptand un electron de la un non-radical, care ramanand cu un electron nepereche devine astfel radical. Ex: radicalul hidroxil oxideaza prometazina, un medicament sedativ care devine radical cation.
![]() PR + OH PR+ + OH
PR + OH PR+ + OH
Un radical poate extrage atomul de hidrogen dintr-o legatura C-H, rezultand un radical al carbonului. De ex. radicalul hidroxil extrage hidrogenul din lantul unui acid gras, initiind peroxidarea lipidica.
![]()
![]()
![]() CH
+ OH C+ H2O
CH
+ OH C+ H2O
Cum cele mai multe molecule biologice sunt non-radicali, formarea unui radical ca cel hidroxil (OH), declanseaza de obicei un lant de reactii. Radicalul carbonului nou format reactioneaza cu O2 cu formarea de radical peroxil care proa reactiile in lant ale peroxidarii lipidelor.
![]()
![]()
![]() C + O2 C-OO
C + O2 C-OO
Radical peroxil
In absenta oxigenului, radicalii carbonil pot forma o legatura covalenta intre ei incheind lantul de reactii
![]()
![]()
![]()
![]()
![]() C
+ C C C
C
+ C C C
3 Stresul oxidativ
Conditii clinice care implica stres oxidativ
Literatura medicala abunda in teorii conform carora radicalii liberi si alte specii reactive sunt implicati in patologia umana. (285, 286) (tabel ). Plaja de afectiuni in care radicalii liberi au o anumita participare cuprinde peste 100 de boli, de la artrita reumatoida si socul hemoragic, pana la cardiomiopatie, cancer etc.
In 1984 unii cercetatori aratau (287) ca marea varietate de afectiuni in care sunt implicate, demonstreaza ca speciile reactive ale oxigenului/azotului (ROS/RNS) sunt o realitate concreta si ca formarea lor in exces insoteste leziunile tisulare din majoritatea bolilor umane, pentru ca aceste leziuni genereaza stres oxidativ (288).
Motivele cresterii stresului oxidativ in agresiunile tisulare, inclusiv eliberarea de ioni ai metalelor tranzitive si ai proteinelor hemale cu rol de catalizator, sau lezarea mitocondriei, sunt sintetizate in ura (289).
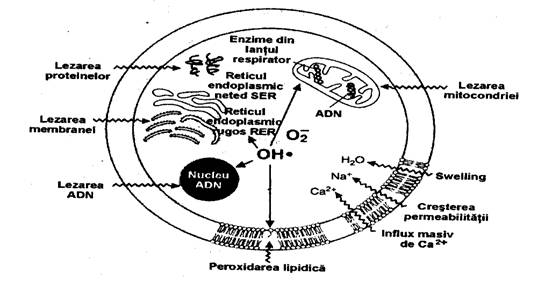
ura 5. Atacul la nivel celular al metabolitilor oxigenului
(dupa M. Greabu Biochimia cavitatii orale. Ed. Tehnica, pg.132, 2001.
Contributia ROS/RNS in patologia bolilor poate fi semnificativa sau nu, de aceea este foarte importanta stabilirea gradului in care aceste substante participa in producerea leziunilor in diferite afectiuni. Pana nu de mult, acest lucru nu era posibil pentru ca lipseau metodele de detectare a radicalilor liberi sau a efectelor acestora asupra tesuturilor, cu aplicabilitate in vivo.
Cercetarile ultimilor 15 ani au pus la punct teste specifice de detectare a ROS/RNS prin metoda capturiisau/si prin determinarea produsilor ce rezulta din stresul oxidativ (ura ).
Criteriile care sustin implicarea semnificativa a radicalilor liberi in producerea leziunilor tisulare intr-o anumita boala sunt:
a) ROS/RNS (sau alt agent) sunt intotdeauna prezenti la locul leziunii;
b) ritmul formari ROS/RNS se suprapune cu ritmul evolutiei leziunii;
c) aplicarea directa a agentului pe tesuturi in vitro, in concentratii similare cu cele gasite in vivo, poate sa reproduca aproape toate leziunile observate in vivo;
d) inlaturarea agentului sau inhibarea formarii lui poate micsora leziunea intr-o proportie ce depinde de gradul inlaturarii/inhibarii agentului lezional
ura . Mecanismele generatoare de stres oxidativ in cursul unor agresiuni tisulare

CATEGORIA
|
EXEMPLE |
|
Afectiuni inflamatorii/autoimune |
Glomerulonefrite, vasculite, boli autoimune, artrita reumatoida hepatite. |
|
Stari de ischemie-reperfuzie |
Accident vascular cerebral, infarct acut de miocard, aritmii cardiace, angina instabila, transt de organ, artrite inflamatorii, degeraturi, contractura Dupuytren. |
|
Reactii induse de toxine si medicamente Supraincarcare cu fier |
Hemocromatoza idiopatica, ingestia excesiva de fier, talasemia sau alte anemii cronice tratate cu transfuzii multiple, alcoolism, insuficienta multiorgan, insuficienta hepatica fulminanta, prematuritatea,chimioterapia si radioterapia din cancer. |
|
Efectele radiatiilor ionizante |
Consecinta exploziilor nucleare, expunerea accidentala., radioterapia, cataracta. |
|
Imbatrinirea |
Tulburarile imbatrinirii premature, bolile batranilor inclusiv cancerul. |
|
Afectiuni ale eritrocitului |
Reactia la medicamente ca phenilhidrazina, primaquina, otravuri, malaria, anemia falciforma, favism, anemia Fanconi, anemia hemolitica a prematurilor, chimioterapia. |
|
Afectarea tractului respirator |
Efectele fumatului, emfizemul, hiperoxia, displazia bronhopulmonara, expunerea la poluanti (ozon, NO2, SO2,), pneumoconieze, carcinogeneza din azbestoza, toxicitatea la bleomicina, paraquat, astmul, fibroza chistica. |
|
Afectiuni cardiovasculare |
Cardiomiopatia alcoolica, boala Keshan, ateroscleroza, supraincarcarea cardiaca cu fier, cardiotoxicitatea antraciclinei. |
|
Afectiuni renale |
Sindrom nefrotic autoimun, nefrotoxicitatea la aminoclicozide, sau la metale grele, hemodializa,, transtul renal. |
|
Afectiuni gastrointestinale |
Leziuni hepatice date de endotoxine sau hidrocarburi halogenate, agenti diabetogeni, pancreatita, gastrite induse de antiinflamatoare, ingestia accidentala de fier. |
|
Afectiuni nervoase si neuromusculare |
Expunere la oxigen hiperbar, sau la neurotoxine, deficienta de vitamina E, b. Alzhaimer, b. Parkinson, coreea Huntingdon, AVC, encefalomielita alergica, supraincarcarea cu aluminiu, traumatismele, distrofia musculara, scleroza multipla, scleroza laterala amiotrofica, dementa Guam. |
|
Afectiuni ale ochiului |
Cataracta, hemoragii oculare, retinopatia degenerativa, retinopatia prematurilor, fotoretinopatia, penetrarea de obiecte metalice. |
|
Afectiuni ale pielii |
Expunerea la radiatii ultraviolete, leziunile termale, porfiria, expunerea la alti fotosensibilizanti, dermite de contact, alopecia |
Tabel . Conditii clinice in care este implicat stresul oxidativ
(dupa Free Rad. Res. Commun. 19, 141 1993)
Producerea de metaboliti activi ai oxigenului este un proces fiziologic care creste in intensitate o data cu varsta, inflamatia, bolile infectioase, expunerea la radiatii, poluanti chimici, mod / stil de viata, acut sau cronic, pe o durata de timp mai lunga (290, 291).
O data formate SRO sunt rapid descompuse de catre sistemele antioxidante enzimatice si neenzimatice existente in celule. Atunci cand acestea sunt depasite de producerea in exces a speciilor active apare asa numitul stres oxidativ, notiune fundamentata de cercetatori din SUA, Anglia, Germania (B Ames (274), B. Halliwell (271), H. Sies (292)), stres care trebuie privit ca un dezechilibru dinamic (. ) si care poate fi definit ca o modificare patologica produsa sub actiunea unui flux puternic de metaboliti activi ai oxigenului, determinata de un dezechilibru intre sistemele de producere ale acestora si cele de protectie antioxidanta endogena.
ura 2. Stresul oxidativ
![]()
![]()
![]() Sisteme
antioxidante
Sisteme
antioxidante
de aparare endogene
si exogene
![]()

![]() specii active
specii active
![]()
![]() ale oxigenului
ale oxigenului
Principalele cauze ale aparitiei stresului oxidativ sunt redate in tabelul 3. stresul oxidativ apare la nivel celular, intr-un organ sensibilizat fie ereditar fie prin reactii de producere de SRO (294).
Tabel 3. Principalele cauze ale producerii stresului oxidativ
|
Tip metabolizare |
Factori favorizanti |
|
1.Cresterea gradului de conversie a oxigenului in superoxid anion |
Radiatii ionizante Reperfuzie Hemoglobine instabile Leucocite activate de procese inflamatorii Compusi chimici |
|
2.Reducerea activitatii enzimelor protectoare |
|
|
3.Prezenta fierului necomplexat in exces |
Intoxicatii cu fier Dereglari in echilibrul vitamina C / vitamina E |
Efectul primar (tabel ) este localizat si reversibil, in functie de intensitatea stresului oxidativ si de nivelul antioxidantilor. Acest efect primar poate dura ani de zile, poate fi compensat sau prelungit. Trecerea la efectul secundar marcheaza faza ireversibila. Daca in etapa primara apar simptome minore, trecerea la efectul secundar se insoteste de aparitia unor manifestari clinice datorate lizei celulare, functiilor alterate, rezistenta scazuta la efort, sau infectii. Starea de boala asociata devine evidenta(295).
5.2. Originea stresului oxidativ
In principiu, bolile asociate stresului oxidativ ar putea rezulta prin una sau ambele dintre urmatoarele modalitati (296):
a) scaderea apararii antioxidante prin mutatii genetice care afecteaza enzimele antioxidante (cum sunt CuZnSOD, MnSOD, glutation-peroxidaza-GPX) sau prin depletia antioxidantilor in cursul evolutiei altei boli.
Multe xenobiotice sunt metabolizate prin conjugare cu glutation (GSH). Excesul de xenobiotice patrunse in organism determina depletia GSH, generand stres oxidativ, chiar daca xenobioticul respectiv nu este in mod direct producator de RNS sau ROS.
b) cresterea productiei de ROS/RNS fie prin expunere la concentratii mari de O2, fie prin prezenta unor toxine care pot fi chiar ele specii reactive (ex.NO2●) sau sunt metabolizate pina la ROS/RNS, fie prin activarea excesiva a sistemelor naturale producatoare de ROS/RNS (de ex.. activarea excesiva a celulelor fagocitare in bolile inflamatorii cronice).
Cel de-al doilea mecanism este mult mai relevant in studierea bolilor si reprezinta tinta interventiilor terapeutice, in timp ce primul mecanism este de obicei neglijat si se acorda prea putina importanta statusului nutritional al pacientilor. De exemplu, pacientii internati in unitati de terapie intensiva au un nivel scazut de ascorbat in plasma iar administrarea lui ar putea fi benefica.(297)
5.3. Consecintele stresului oxidativ
Stresul oxidativ poate determina:
a) adaptarea prin suprareglarea sistemului de aparare antioxidant, care realizeaza:
protectie completa impotriva leziunilor;
protectie incompleta impotriva leziunilor;
supraprotectie celulele devenind rezistente la nivele inalte ale stresului oxidativ, impus subsecvent in prealabil;
Un exemplu de adaptare incompleta se obtine prin expunerea graduala a unor sobolani adulti la nivele crescute de O2, dupa care sunt expusi la oxigen pur; ei rezista mai mult decat lotul-control la expunerea in atmosfera de oxigen pur, datorita cresterii sintezei enzimelor antioxidante si a glutationului in plaman. Leziunile determinate de stresul oxidativ sunt in acest caz incetinite, nu prevenite.
Tabel Consecinte biologice ale stresului oxidativ
|
Efect primar reversibil |
Modificari ale permeabilitatii membranei celulare, dezechilibrul ionic Peroxidarea acizilor grasi din membranele celulare Modificarea unor procese metabolice celulare datorita alterarii unor proteine Scaderea producerii de energie |
|
Efect secundar ireversibil |
Dezechilibrul ionilor de calciu care favorizeaza activarea enzimelor hidrolitice, protease Lize celulare Tulburari de circulatie sanguina Peroxidarea proteinelor, acizilor nucleici Alterari ale reactivitatii immune Distrugeri tisulare localizate intr-un organ sau mai multe |
Un alt experiment evidentiaza adaptarea la stres oxidativ prin supraprotectie: tratarea unor colonii de Escherichia coli cu concentratii scazute de H2O2 creste transcriptia genei responsabile de sinteza unei proteine protectoare, asfel incat bacteria devine rezistenta la concentratii mari de H2O2.
Exemplele de adaptare prin supraprotectie la animale sunt mai rare, dar unul recent a fost oferit de experimente ce vizeaza ischemia preconditionata (298): o scurta perioada de ischemie produsa pe inima de porc duce la scaderea contractilitatii, care se amelioreaza la administrarea de antioxidanti. Repetarea episoadelor de ischemie duce la o revenire rapida a contractilitatii cardiace la animalele netratate cu antioxidanti, dar absenta acestei reactii de adaptare la animalele tratate. Cu alte cuvinte, stresul oxidativ produs de ischemie-reperfuzie produce initial unele tulburari, dar determina totodata si un raspuns protector impotriva expunerii subsecvente la ischemie-reperfuzie.
b) Lezarea tesuturilor. Stresul oxidativ poate afecta toate moleculele organice ale celulei, care devin tinta leziunilor : ADN, proteine, lipide, carbohidrati. Perspectivele pentru o interventie terapeutica eficace pot esua, daca nu se cunoaste tinta initiala a stresului oxidativ. De exemplu, se stie ca ADN este tinta initiala a leziunilor produse de adaugarea H2O2 in culturi celulare de mamifer, astfel incit rupturile lantului de ADN apar inaintea peroxizilor lipidici detectabili sau a proteinelor oxidate detectabile. Metoda de detectare a leziunilor produse asupra unor molecule tinte poate da informatii incomplete; astfel, evidentierea lezarii proteinelor prin detectarea radicalilor carbonil in stadii initiale ale leziunilor poate fi negativa, dar determinarea oxidarii guparilor SH, care se produce mai precoce, este pozitiva.
In general, peroxidarea lipidelor apare in stadii tardive ale agresiunii, astfel incat terapiile indreptate impotriva lipoperoxidarii pot fi mai putin benefice. Acesta este inca un motiv care poate conduce la concluzii eronate privind importanta stresului oxidativ si a terapiilor antioxidante.
c) Moartea celulara. In general, moartea celulara se produce prin doua mecanisme esentiale, care implica stres oxidativ: necroza si apoptoza.
In moartea celulara necrotica celulele balonizate si rupte isi elimina continutul in jur afectand celulele vecine. Ele pot contine antioxidanti ca: glutation, catalaza si prooxidanti ca: ionii de fier, cupru si proteinele hemale .( ura )
ura . Semnificatia stresului oxidativ in evolutia bolii
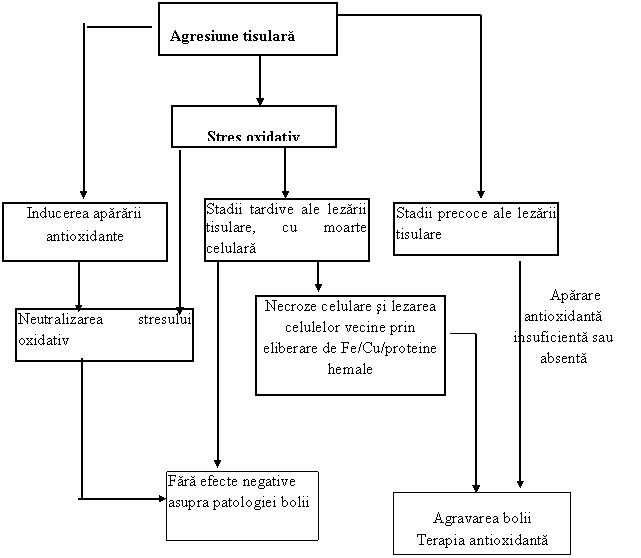
Astfel, chiar daca moartea celulelor s-a produs prin alt mecanism decat stresul oxidativ, moartea celulara necrotica creaza stres oxidativ asupra tesuturilor adiacente.
In apoptoza sunt activate mecanismele celulare intrinseci de sinucidere sau moarte programata, astfel incat celulele moarte prin apoptoza nu isi elibereaza continutul si nu afecteaza tesuturile din jur. Totusi, in anumite conditii patologice, cum sunt bolile neurodegenerative, apoptoza poate fi accelerata, generand stres oxidativ.
Cercetarile recente arata ca cele doua mecanisme de moarte celulara sunt extreme si ca, in celulele care mor se intalnesc elemente din ambele mecanisme.
Se pune intrebarea fireasca: daca ROS/RNS se produc in cantitate mare in majoritatea bolilor, au ele o contributie semnificativa in patologia bolilor sau consecintele formarii lor sunt minime/absente? Se pare ca raspunsul difera de la o boala la alta. (ura )
Pentru a demonstra ca ROS/RNS sunt implicate intr-o anumita boala, este necesara indeplinirea celor patru criterii enumerate in submodulul , folosind teste de determinare a biomarkerilor cei mai relevanti pentru boala respectiva. (ura )
5. Semnificatia stresului oxidativ in bolile umane
Unele boli umane pot fi cauzate direct de stresul oxidativ. De exemplu, radiatiile ionizante genereaza OH● prin scindarea moleculei de apa, astfel incat majoritatea consecintelor biologice determinate de expunerea excesiva la radiatii sunt produse de leziunile oxidative ale proteinelor, lipidelor si ADN. Simptomele produse de carenta cronica de seleniu alimentar (B.Keshan) sau tocoferol (tulburari in absorbtia intestinala a grasimilor alimentare), ar putea fi mediate de asemenea, de stresul oxidativ. Multi autori atribuie cardiomiopatia observata in boala Keshan, absentei glutation-peroxidazei, care genereaza o indepartare insuficienta a peroxidului de hidrogen (H2O2) si acumularea peroxizilor lipidici. Desi nu exista do certe ca acesta este mecanismul leziunilor tisulare, pacientii ce sufera de b. Keshan au un nivel scazut al GPX-dependenta de seleniu, atat in sange cat si in tesuturi.
In foarte multe afectiuni umane, stresul oxidativ este doar o consecinta, nu o cauza a procesului patologic al bolii. Lezarea tesuturilor de catre agenti agresori ca: infectii, traumatisme, toxine, temperaturi extreme, etc., duce la supraproductia unor mediatori ai leziunilor ca: prostaglandine, leucotriene, interleukine si citokine (ca factorul tumoral al necrozei TNF), care joaca un rol important in producerea leziunilor tisulare.(299) Din aceeasi categorie de mediatori ai leziunilor fac parte si ROS/RNS inclusiv NO2● (ura 1) ( 300).
De exemplu, cresterea peroxidarii lipidelor, demonstrata la pacientii cu distrofie musculara (301) pare sa fie o consecinta a leziunilor, fara a avea vreo contributie la producerea lor, astfel incat administrarea de antioxidanti nu pare sa fie benefica. Un alt exemplu, infectia celulelor endoteliale umane cu Rickettia rickettsii-agentul cauzal al unei boli febrile, determina o crestere a peroxizilor lipidici (302), dar inhibarea peroxidarii nu previne agresiunea microorganismului asupra celulelor umane. Aceste date arata ca peroxidarea lipidelor nu este importanta in cele doua cazuri, dar nu exclude stresul oxidativ printr-un alt mecanism.
ura . Biomarkeri ai strexului oxidativ ce pot fi utilizati in studiul bolilor
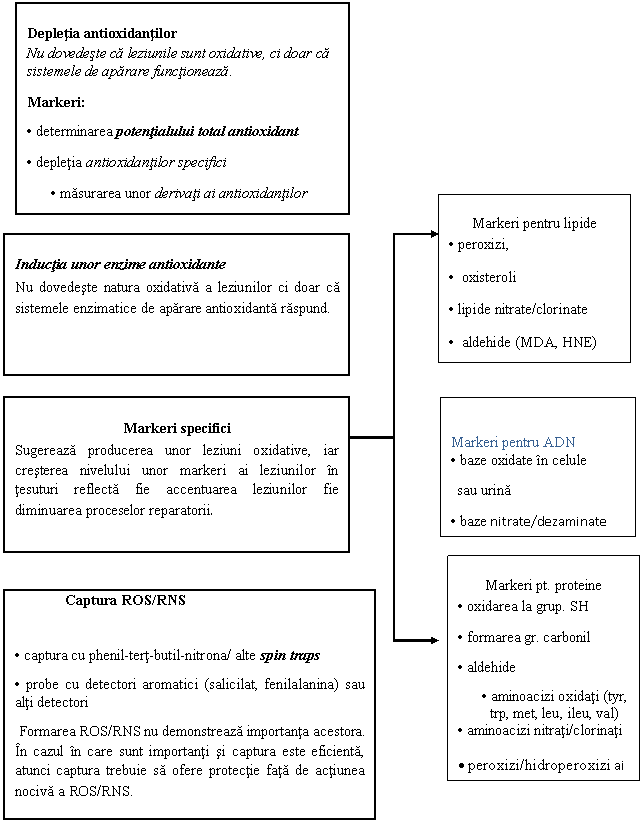
Speciile reactive ale oxigenului (ROS) sunt esentiale pentru viata din cauza rolului indeplinit in multe procese vitale cum ar fi transductia informatiei intercelulare si abilitatea fagocitelor de a-si indeplini activitatea bactericida. ROS includ radicali liberi, cum sunt radicalii hidroxil si superoxid, care sunt substante cu unul sau mai multi electroni pe orbita cu status de spin nepereche, si substante neradicali liberi, cum sunt peroxidul de hidrogen si oxigenul singlet (303, 304, 305). Desi productia de ROS este strict controlata de procese fine de reglare, pentru functiile lor esentiale, in multe procese celulare sunt generati ROS. Un loc important de generare a acestor ROS nonesentiali, ceea ce constituie stresul oxidativ, este in sistemul transportor de electroni CETS ( ura ), care isi are sediul la nivelul membranei interne a mitocondriei.
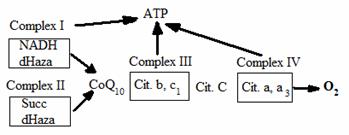
ura Sistemul transportor de electroni. Electronii trec de la Complexul I (NADH-dihidrogenaza) si complexul II (Succinat-dihidrogenaza) la Coenzima Q10, apoi la Complexul III (citocromul b si c1) apoi Citocromul c Complexul IV. Transferul final este a 4-electroni catre oxigen, cu formarea de apa. Sistemul transportor de electroni este cuplat la 3 nivele cu fosforilarea oxidativa, ceea ce determina formarea ATP-ului (adenosine-trifosfatul).
In mod natural, electronii sunt transferati de la Complexul I si complexul II la CoQ10 si apoi la Complexul III citocromul c si Complexul IV. In final 4 electroni sunt transferati la oxigen, cu formarea de apa. In acest proces, cuplarea transportului de electroni la fosforilarea oxidativa are ca rezultat generarea de adenozina-trifosfat (ATP). Desi acest proces este foarte eficient, aproximativ 2% din electroni scapa din ETS si reactioneaza cu oxigenul molecular pentru a forma radicali superoxid. Desi superoxidul nu este foarte toxic, superoxid-dismutaza mitocondriala genereaza peroxid de hidrogen din radicalii superoxid, si, in prezenta fierului sau cuprului redus, via reactiile Fenton sau Haber-Weiss se formeaza radicalul hidroxil cu o inalta toxicitate. Sistemul citocrom P450 monoxidaza din microzomii reticulului endoplasmic hepatic, genereaza, de asemenea, o cantitate substantiala de ROS in procesele de metabolizare a diferitilor compusi chimici pe care ii administram ca medicamente, alimente sau substante din mediul ambiant. Plasma si membranele nucleare sunt locuri mai putin active de generare a ROS si sistemele enzimatice cum ar fi xantin oxidaza, pot genera ROS.
ROS interactioneaza cu macromoleculele celulare inclusiv ADN, proteine si lipide, interferand cu formatii celulare vitale. Mutatiile determinate de ROS pot determina transformari maligne si dezvolta cancer, ca si o multime de alte boli degenerative inclusiv imbatranirea. In conditii normale mecanismele antioxidante, incluzand antioxidantii cu greutate moleculara mica si sisteme enzimatice antioxidante, curata ROS si protejeaza organismul de stresul oxidativ.
Stresul oxidativ este definit ca o stare in care nivelul intermediarilor reactivi toxici ai oxigenului depaseste sistemele endogene antioxidante de aparare ale gazdei. Stresul oxidativ poate rezulta, astfel, fie dintr-o productie in exces de oxidanti, fie dintr-o deplectie a antioxidantilor de aparare.
ROS sunt produsi ca un rezultat al proceselor fiziologice normale, inclusiv pierderea de electroni din lanturile de transfer de electroni celulare si ca produsi secundari ai metabolismului lipidelor membranare .
In cazul bolii, ROS sunt produse de celulele fagocitare ca un mecanism de distrugere a microorganismelor invadante. Cand inflamatia devine sistemica, ca in sindromul de raspuns inflamator sistemic (SIRS) sau in sepsis, pierderea controlului productiei de ROS poate conduce la o lezare nediscriminatorie a tesuturilor invecinate ale gazdei. ROS determina lezarea directa celulara prin injurie oxidativa a proteinelor si acizilor nucleici celulari, dar si prin inducerea peroxidarii lipidice, ceea ce conduce la distrugerea membranelor celulare.
Complementar citotoxicitatii directe, ROS joaca rol si de mesageri secundari ai cailor de transmisie intracelulara a semnalelor pentru celulele inflamatorii. In mod particular, activarea factorului critic nuclear de transcriptie, factorul nuclear kB(NF-kB) s-a dovedit a fi indusa de peroxidul de hidrogen si blocata de cativa antioxidanti, inclusiv vitamina E (306), (307). Factorul nuclear kB este un factor de transcriptie central implicat in reglarea a numeroase gene proinflamatorii, inclusiv a multor citokine (TNF-tumor necrosis factor, interleukina: IL-l, IL-6, IL-8, IL-2), factori de crestere hematopoetici (factorul de stimulare a coloniilor de granulocite-macrofage, factorul de stimulare a coloniilor de macrofage, factorul de stimulare a coloniilor de granulocite), a moleculelor de adeziune celulara (CAM) CAM-l intercelulare, molecula-l de adeziune a sintazei oxidului nitric (INOS) (308). Factorul nuclear kB a fost demonstrat ca un important mediator al transductiei semnalului pentru activarea citokinelor indusa atat de endotoxina cat si de inflamatie. Un al doilea factor major al transcriptiei, proteina activatoare 1 (AP-l), de asemenea, pare a fi reglata de schimbari ale statusului redox al celulelor si poate fi activata atat de oxidanti, cat si de antioxidanti, in functie de tipul celulei si de conditiile intracelulare (309), (310), (311). In plus, cateva gene inflamatorii au situsuri promotorii pentru AP-l, desi rolul sau in semnalele inflamatorii este mai putin documentat decat pentru NF-kB. Astfel alterarea statusului redox al celulei poate contribui la perpetuarea producerii de citokine inflamatorii si la progresia sindromului de raspuns inflamator sistemic (SIRS), conducand la leziuni organice. Acestea se pot manifesta prin dezvoltarea unui sindrom de disfunctie respiratorie acuta (ARDS) sau ca un sindrom de disfunctie organica multipla (MODS).
In plus de sindromul inflamator sistemic stresul oxidativ a fost implicat in manifestarile altor cauze comune de afectiuni critice: leziunile de ischemie si reperfuzie. Ischemia tesuturilor urmata de reperfuzia cu sange oxigenat, in timpul resuscitarii, conduce la o productie semnificativa de ROS. Aceasta este amorsata de cresterea activitatii xantin-oxidazei si cresterea productiei de hipoxantina datorita pierderii de adenozin-trifosfat in timpul ischemiei. Cand oxigenul este reintrodus exista o crestere atat a substratului cat si a activitatii enzimei pentru urmatoarea reactie:
Xantina sau Hipoxantina + H2O + 2O2 acid uric + 2O2- + 2H+.
Ischemia si leziunile de reperfuzie, apar la nivel sistemic, in timpul socului hipovolemic si resuscitarii. De asemenea, apar la nivel local, in cateva scenarii clinice, in cazul ischemiei unui membru cu revascularizare sau fasciotomie, in infarctul miocardic cu tromboliza si dupa transtul unui organ.
Pentru a combate amenintarea stresului oxidativ, exista un numar mare de sisteme endogene antioxidante. Acestea includ vitaminele E si C, provitamina A (b - carotenul), glutationul, superoxid dismutaza si catalaza, bilirubina, uratul si alte proteine plasmatice. Acesti antioxidanti pot fi impartiti in doua grupe: enzimatici si nonenzimatici
Tabel Apararea antioxidanta
ENZIMATICI NONENZIMATICI
Superoxid dismutaza Vitamina E
Catalaza Vitamina C
Glutation peroxidaza Vitamina A/β caroten
Glutationul
Bilirubina
Uratul
Antioxidantii enzimatici includ: superoxid dismutaza care catalizeaza conversia O2- la H2O2 sau H2O; catalaza, care converteste apoi H2O2 la H2O si O2; si glutation-peroxidaza, care reduce H2O2 la H2O prin oxidarea glutationului (GSH). Re reducerea formei oxidate a glutationului (glutation-dinilfidul) este apoi catalizata de glutadion reductaza. Aceste enzime necesita, de asemenea, cantitati mici de metale cofactori pentru a avea eficienta maxima, incluzand seleniul pentru glutation peroxidaza; cuprul, zincul sau manganul pentru superoxid dismutaza si fierul pentru catalaza.
Antioxidantii neenzimatici includ: vitaminele liposolubile (vitamina E si vitamina A sau b-carotenul) si vitamine hidrosolubile (vitamina C si glutationul). Vitamina E a fost descrisa ca antioxidantul major la oameni (312), (313). Vitamina E este, de fapt, un termen generic, descriind o colectie de tocoferoli si tocotrienoli obtinuti din uleiuri vegetale. Cel mai activ biologic este a-trocoferolul. Din cauza liposolubilitatii vitamina E este localizata in membranele celulare unde intrerupe peroxidarea lipidica si joaca un rol in modularea cailor de transmisie intracelulara pe care se bazeaza ROS (314). Vitamina E poate stinge (inabuse) si direct ROS, inclusiv O2-, HO si O2. Vitamina A este un termen care cuprinde o colectie de retinoizi obtinuti in dieta in principal din oua, ficat si cereale integrale. b-carotenul este gasit intr-o varietate de fructe si legume si reprezinta cam 25% din vitamina A intr-o dieta occidentala. b-carotenul din dieta este convertit la retinol la nivelul mucoasei intestinale si functioneaza ca un antioxidant intrerupator al lantului.
Vitamina C (acidul ascorbic) obtinut in principal din citrice, functioneaza ca un antioxidant hidrosolubil capabil sa curete pe scara larga ROS, inclusiv oxidantii majori ai neutrofilelor: HO, H2O2 si acidul hipocloros. In anumite circumstante, vitamina C s-a demonstrat ca are proprietati pro-oxidante. De exemplu, cand este combinata cu fierul, s-a demonstrat ca accelereaza peroxidarea lipidica, ceea ce conduce la lezarea membranelor celulare (315).
In sfarsit, glutationul (GSH), care este sintetizat intracelular din cisteina, glicina si glutamat, este capabil sa curete ROS fie in mod direct, fie enzimatic, via glutation-peroxidaza . In plus, glutationul este crucial in mentinerea enzimelor si altor componente celulare intr-o stare redusa. Majoritatea GSH este sintetizat in ficat, si aproximativ 40% este secretat in bila.
Interactiunea intre antioxidanti: ROS induc peroxidarea lipidelor din membranele celulare, rezultand o reactie in lant, care poate fi intrerupta prin curatarea directa a radicalilor peroxil-lipidici de catre vitamina E si b-caroten.Atat vitamina C, cat si glutationul pot apoi recicla vitamina E. Abilitatea de a reduce a GSH este catalizata de enzima glutation peroxidaza. Glutadionul este apoi reciclat de NADPH, care este facilizat de glutation-reductaza.
Sistemele antioxidante enzimatice si nonenzimatice sunt intim legate unul de celalalt. Atat vitamina C cat si GSH sunt implicate in reciclarea radicalilor a-tocoferolului. In plus, oligoelementele seleniu, mangan, cupru si zinc joaca un important rol ca si cofactori antioxidanti nutritionali. Seleniul este un cofactor pentru enzima glutation peroxidaza, iar manganul, cuprul si zincul sunt cofactori pentru superoxid dismutaza. Zincul actioneaza, de asemenea, pentru stabilizarea pool-ului celular metalothioneinic, care are capacitatea de a atenua direct radicalii liberi.
Numeroase studii au evaluat statusul oxidativ sistemic la pacientii critici sau cu diferite forme de leziuni. Astfel, s-a demonstrat cresterea nivelului seric ai produsilor secundari ai peroxidarii lipidelor din membrane la pacienti in stare critica de diverse etiologii (316) (317), (318). De asemenea, s-a dovedit cresterea activitatii oxidative la nivel pulmonar, la pacientii cu sindrom de detresa respiratorie acuta (ARDS) manifestata prin cresterea activitatii mieloperoxidazei si detectarea produsilor de peroxidare lipidica in lichidul de spalare bronhoalveolar (319). Masurarea capacitatii de aparare antioxidanta a dovedit clar scaderea nivelului de vitamina E si C la pacientii cu sepsis si ARDS(315, 316, 317, 318); (320, 321, 322, 323). S-a demonstrat, de asemenea, ca nivelele scazute serice ale vitaminei C, pot avea valoare predictiva pentru dezvoltarea MOFS (Multiple Organ Failure Sindrome) la pacientii cu risc ( 324). Similar valorile glutationului sunt scazute la pacientii cu insuficienta hepatica, la pacientii politraumatizati si la cei cu ARDS in lichidul bronhoalveolar (319), (325, 326).
Un studiu care masoara statusul antioxidant total al plasmei, aplicat la cateva categorii de pacienti cu stare critica, se bazeaza pe inhibarea de catre antioxidantii serici a absorbtiei radicalului cationic 2,2-azino-bis-(3-etilbenzo-tiazolin -6-acid sulfonic) ABTS. Studiile au avut rezultate mai putin transante dar, per total, sustin prezenta unui stres oxidativ sistemic si o depletie a apararii antioxidante la pacientii critici.
8.Rolul mecanismelor moleculare in efectele radioterapiei
Progresele realizate de fiziologia moleculara au modificat radical gandirea medicala si modul de abordare al efectelor iradierii asupra tesuturilor normale. Conceptul clasic al celulei tinta a fost inlocuit de conceptul privind sistemele de celule care interactioneaza stergand diferentele dintre instalarea acuta si cea tardiva a efectelor. Vechea perioada de latenta considerata de saptamani sau luni este acum inlocuita de modelul de transmitere a mesajelor intercelulare : autocrin, paracrin si endocrine, aceasta fiind calea de comunicare intre celulele epiteliale, endoteliale, fibroblatice, monocite, mastocite si celulele imune specifice.
Modularea acestor mesaje se realizeaza prin procese multiple:
reprogramarea genetica a ciclului celular
eliberarea unor factori de crestere sau inhibitori
alterari ale receptorilor celulari specifici care primesc aceste semnale
rezultantele acestor mesaje alterate, care sunt transductiile si translocatiile din nucleu .
[68, 69]
Cheia intelegerii comportamentului special al pacientilor cu neoplazii tratate preoperator radio-chimioterapic o reprezinta principiile sustinute de abordarea schimbata a fiziopatologiei efectelor injuriilor de etiologii diverse asupra tesuturilor normale.
Primul principiu este schimbarea tintei agresiunii de la conceptia celulara spre comunicarea intercelulara conversatia citokinelor .
Al doilea principiu schimbat este cel al circulatiei celulelor inflamatorii si imune si in afara campului de iradiere ele fiind responsabile de efectele tardive asupra tesuturilor normale din afara zonei de agresiune.
Al treilea principiu modificat este cel al recunoasterii sensibilitatii sau rezistentei la efectele toxice ale iradierii datorate tocmai exacerbarii sau atenuarii raspunsului citokinelor care moduleaza reactiile organismului la agresiune.
Cancerul si terapiile antineoplazice reprezinta adevarate provocari pentru anestezist .In completarea cunostintelor despre neoplazie si extinderea sa, acesta trebuie sa inteleaga implicatiile diferitelor modalitati de terapie antineoplazica, efectele cumulate, durata si evolutia in timp a efectelor secundare.
Studiile specifice asupra interactiunii directe anestezie terapie antineoplazica sunt putine si destul de superficiale, dar abordarea dintr-un unghi comun - cel al sistemului mesagerial al citokinelor si al efectorilor lor la nivel intracelular, radicalii liberi, modulatorii raspunsului organismului la orice fel de agresiune- poate fi solutia optima de intelegere si optimizare a ingrijirii perioperatorii a pacientilor neoplazici.
In tesuturile expuse iradierii se produc radicali liberi citotoxici si stres oxidativ extensiv (327, 328). Radiatiile ionizante produc un numar de specii reactive ale oxigenului, incluzand ionul superoxid, radicalul hidroxil si peroxidul de hidrogen. In mod curent, se postuleaza ca efectele terapeutice primare ale radioterapiei sunt mediate de generarea speciilor reactive citotoxice ale oxigenului.(327, 329). Radicalii hidroxil sunt generati de radiatiile ionizante fie dirct prin oxidarea apei, fie indirect , prin formarea de specii reactive ale oxigenului secundari. Acestia pot fi ulterior convertiti la radicali hidroxil, activare datorata proceselor metabolice din celule. Injuria secundara iradierii este astfel influentata de statusul antioxidant celular si de cantitatea si biodisponibilitatea mecanismelor activate. Raspunsul biologic la iradiere poate fi modulat prin alterarea factorilor care influenteaza aceste mecanisme secundare ale injuriei celulare.(330)
In plus, celulele canceroase acumuleaza fier, iar radioterapia creste concentratia intracelulara de fier liber, care poate ducela producerea de radicali hidroxil citotoxici, prin intermediul reactiei Fenton( 331). Celulele expuse la radioterapie sunt supuse unui stres oxidativ. Aceste celule fie se adapteaza acestor conditii,fie mor. Adaptarea include adesea inducerea activarii unor cai biochimice care sa atenueze sau sa distruga intermediarii reactivi toxici. Astfel, s-a observat in celulele de glioblastom uman U 251 ca radiatiile au indus supraexpresia unui numar de enzime antioxidante, inclusiv superoxid dismutaza ( de 2 ori ) si glutation peroxidaza ( de 5 ori) (330, 332).
Stresul oxidativ asociat cu tratamentul policitostatic
Agentii antineoplazici au fost dovediti ca producatori de stres oxidativ la pacientii care au primit aceste substante in cadrul chimioterapiei antineoplazice ( 333, 334, 335, 336, 337, 338, 339,340, 341). Acest lucru este evidentiat prin cresterea serica a produsilor de peroxidare lipidica; prin scaderea capacitatii totale a plasmei de a capta radicali liberi; prin scaderea nivelelor plasmatice ale antioxidantilor cum ar fi vitamina E, vitamina C si b-carotenul; si, mai ales, prin scaderea marcata a nivelelor tisulare ale glutationului care apare in cursul chimioterapiei. Agentii citostatici care genereaza nivelele foarte inalte de ROS sunt: antraciclinele (doxorubicina, epirubicina si daunorubicina), agentii alkilanti, complexele legate de platina (cisplatin, carboplatin, oxaliplatin), camptotecine (topotecan, irinotecam) si epipodofilotoxinele (etoposide si teniposide).
|
Stresul oxidativ si chemoterapia |
||
|
Stresul oxidativ si chimioterapia.
Cele mai inalte nivele de stres oxidativ indus de agentii antineoplazici sunt date de antracidine. Aceasta se datoreaza abilitatilor unice de a genera specii reactive ale oxigenului (ROS) in mitocondria fibrelor miocardice. Complexele legate de platina, agentii alkilanti, epipodofilotoxinele si camptotecanii genereaza, de asemenea, stres oxidativ la nivelul mai multor site-uri celulare. Nucleozidele si analogii nucleotidelor, antifolanii, taxanii si vinka-alcaloizii genereaza numai nivele scazute de stress oxidativ, care apare in primul rand ca urmare a apoptozei induse de chimioterapie.
Antraciclinele genereaza de departe, cele mai crescute nivele de stres oxidativ. Acesta se datoreaza abilitatii lor de a devia electroni de la nivelul ETS (sistemul transportor de electroni) al mitocondriilor fibrelor miocardice, rezultatul fiind formarea de radicali superoxid (342) si, in plus, de a genera ROS la nivelul altor site-uri celulare. Doxorubicina, cea mai studiata antraciclina, poseda o parte de zaharid atasata unui inel tetraciclinic, care contine o structura chinonica. Scindarea ETS de catre doxorubicina poate apare numai dupa reducerea chinonei la semichinone. Doxorubicina este hidrofila, iar in mitocondriile majoritatii celulelor ea nu poate penetra membrana interna si sa fie redusa de dihidrogenaza-NADH (complexul I), care este localizata pe suprafata interna (matriceala) a membranei mitocondriei. Totusi, structura membranei interne a mitocondriei fibrei miocardice este unica, in sensul ca aceasta poseda o dehidrogenaza-NADH pe suprafata externa(citozolica) in plus de dehidrogenaza-NADH matriceala prezenta in mitocondriile celorlalte celule (343). In fibrele miocardice, doxorubicina poate penetra membrana mitocondriala externa si intra in citozol unde este redusa de dehidrogenaza-NADH citozolica. Rearanjarea intramoleculara rezulta in formarea de derivat deoxiaglicon-lipofolic al doxorubicinei, care penetreaza membrana interna. Aici intra in competitie cu coenzima Q10 (ambele avand structura chinonica) ca si acceptori de electroni, deviind electronii catre oxigenul molecular, cu formarea de radicali superoxid.
In contrast cu grupul descris de chimioterapice, taxanii (ex. paclitaxel si drectaxel), alcaloizii de vinka (vincristine, vinblastine), antimetabolitii, nucleozidele si analogii nucleotidelor, genereaza doar nivele scazute de stres oxidativ. Totusi, toate drogurile antineoplazice genereaza ROS deoarece induc apoptoza in celulele neoplazice. Aceasta, deoarece, una din caile de inducere a apoptozei pe cale medicamentoasa, implica eliberarea de citocrome c din mitocondrie (344, 345). Cand are loc acest fenomen electronii sunt deviati din ETS spre oxigen, de catre dihihrogenaza NADH si coenzima Q10 redusa, rezultatul fiind formarea de radicali superoxid.
Stresul oxidativ interfera cu procesele celulare (progresia ciclului celular si apoptoza drog indusa) ceea ce este necesar pentru agentii antineoplazici pentru a-si exercita citotoxicitatea optima asupra celulelor neoplazice, iar nivelele modeste ale stresului oxidativ s-a dovedit ca reduc citotoxicitatea drogurilor citostatice (346). Astfel, formarea de ROS care are loc in momentul administrarii chimioterapicelor antineoplazice, poate diminua eficienta tratamentului. In plus, odata ce unele efecte secundare determinate de citostatice par sa fie prevenite de anumiti antioxidanti, administrarea acestor suplimente in timpul chimioterapiei poate diminua dezvoltarea de efecte secundare ca si imbunatatirea raspunsului la terapie. Aceste supozitii sunt sustinute de multe studii preclinice, dar si cateva clinice (347, 348).
Radicalii liberi generati in timpul stresului oxidativ au multe tinte celulare desi una dintre primele tinte sunt lipidele celulare. Peroxidarea lipidica a acizilor grasi polinesaturati are ca rezultat formarea de radicali peroxil si alkoxil. Acesti produsi primari ai peroxidarii lipidice, care sunt foarte reactivi si au o viata foarte scurta, sunt supusi in continuare altor reactii pentru formarea unor produsi secundari ai peroxidarii lipidice, care includ o varietate de aldehide (TABEL 1), cum sunt malondialdehida, 4-hidroxialkenalii si acroleina (349). Aldehidele sunt mai stabile decat produsii primari si pot difuza in intreaga celula, unde lezeaza componentele celulare si interfera cu functiile celulare. Din cauza caracterului lor electrofil, aldehidele se leaga de grupul nucleofilic de aminoacizi, cum sunt cisteina, lizina, bistidina, serina si tirozina, care sunt componente esentiale ale situsurilor enzimatice active sau sunt necesare pentru mentinerea structurii tertiare a proteinelor. Legarea aldihidelor de proteine, care determina inhibitia enzimatica si alterarea structurii receptorilor celulari, poate explica impactul stresului oxidativ asupra citotoxicitatii agentilor antineoplazici
Ciclul celular (. 3 .) este format din 4 faze: G1, S, G2 si M. In timpul fazei G1, celula se pregateste pentru sinteza ADN-ului. Faza S este faza de sinteza a AND. In timpul fazei G2, celula se pregateste pentru mitoza. Faza M este faza mitozei, in timpul careia celula se divide in doua celule fice.
Punctele de reglare si de siguranta majore ale ciclului celular includ punctul de restrictie (R) si punctele de control (C). O particularitate fundamentala a unui ciclu celular normal este controlul strict al deciziei celulei de a avansa spre o alta runda de sinteza a ADN-ului. In prezenta de agenti mitogeni si alte necesitati indeplinite, cum ar fi prezenta de nutrienti, celula va trece de punctul de restrictie si se va supune unui alt ciclu de sinteza a ADN. Punctele de control, care asigura faptul ca integritatea genomului e mentinuta, sunt plasate in G1 si G2,acestea oprind ciclul celular daca sunt detectate lezari ale ADN-ului; punctul de control din faza S, opreste ciclul celular daca apar probleme cu replicarea ADN-ului; si punctul de control al fazei M, care opreste ciclul celular daca apar probleme cu formarea fusului de diviziune mitotica. Cand ciclul celular se opreste la un punct de control, celula fie este capabila sa corecteze defectul ce a fost detectat (ex. prin repararea ADN), fie se supune apoptozei.
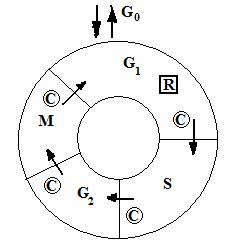
. .Ciclul celular
Stresul oxidativ scade rata proliferarii celulare prin inhibarea tranzitiei de la faza G0, la faza G1 a celulelor, prelungind faza G1, incetinind progresia spre faza S prin inhibarea sintezei ADN, inhiband progresia ciclului celular prin punctul de restrictie si determinand oprirea ciclului celular in punctele de control (350,351,352). Astfel, rata poliferarilor celulare in culturi (de celule normale sau de celule neoplazice) descreste in timpul episoadelor de stres oxidativ (353, 354, 355), iar stresul oxidativ incetineste cresterea tumorilor la animalele de laborator (356,357), 4-hidroxialchenarii, in mod specific, s-a dovedit ca inhiba cresterea celulelor tumorale in culturi(358) si la animale de laborator . Alte studii demonstreaza clar ca o rata de crestere inalta atat a tesuturilor normale (ficat) (359), dar si tumorale (360), se asociaza cu un nivel scazut al peroxidarii lipidice. Astfel nu este deloc surprinzator faptul ca celulele tumorale au nivel diminuat al enzimelor pro-oxidante si sisteme eficiente antioxidante, astfel incat pot mentine un nivel scazut al stresului oxidativ intracelular si o rata inalta a proliferarii (361,362,363,364,365).
Efectele stresului oxidativ asupra proliferarii celulare sunt cel mai probabil atribuibile inhibarii enzimelor critice de catre aldehide si inhibarii selective a ADN-polimerazei de 4-bideoalkenali, asa cum a fost demonstrat, prin multe studii (366, 367, 368, 369). Kinazele ciclin-dependente (CDK)sunt alte tinte ale aldehidelor. Aceste enzime asigura progresia programata spre fazele ciclului celular, iar inhibarea lor, de exemplu, de catre inhibitorul CDK p 21 (mediatorul genei de supresie tumorala p 53, previne trecerea prin punctul de restrictie si determina oprirea in punctele de control.
Agentii antineoplazici, care dezvolta activitatea specifica asupra ciclului celular, depind de progresia ciclului celular pentru a-si exercita activitatea antineoplazica, iar interferenta cu aceasta progresie, va diminua citotoxicitatea drogurilor. Exemple de agenti antineoplazici care isi exercita actiunea in faze specifice ale ciclului celular sunt:
1) antiaciclinele si epidofolotoxinele care inhiba activitatea topozinerazei II si actioneaza in faza S,
2) antifolatii si analogii de nucleotide/nucleozide care interfera cu sinteza ADN-ului si actioneaza in faza S,
3) alcaloizii de vinka si taxanii care interfera cu procesele nitrozei si actioneaza primordial in faza M,
4) camptotecanii care inhiba topoizomeraza I, actioneaza in faza S.
Chiar si complexele dependente de platina si agentii alkilanti, care nu sunt considerati dependenti de ciclul celular, au nevoie de progresia celulelor din faza S si faza G2 pentru a induce apoptoza. In plus, repararea ADN-ului lezat de complexele de platina si agentii alkilanti conduce la ezistenta la aceste droguri, iar oprirea in punctele de control in timpul stresului oxidativ, poate exacerba procesele de reparare si diminua eficienta tratamentului . Din acest punct de vedere, revocarea punctelor de control, opusul a ceea ce se intampla in timpul stresului oxidativ, s-a dovedit ca mareste citotoxicitatea celor mai multe droguri antineoplazice.Prin scaderea generarii aldehidelor, antioxidantii pot contracara efectele stresului oxidativ indus de drogurile chimioterapice asupra ciclului celular si astfel, pot spori citotoxicitatea agentilor antineoplazici.
Cele doua cai majore de inducere a apoptozei prin droguri sunt: calea mitocondriei, initiata de citocromul c si calea receptorului mortii CD95, initiata de legarea receptorului de ligantul sau CD95L (370). In continuarea momentului de initiere, procesele apoptotice sunt duse mai departe de o familie de enzime numite caspaze(371, 372, 373). Caspazele (proteaze cistein-dependente controlate de aspartat sunt proteaze care au un reziduu de cisteina la situsul activ si necesita un mediu reductor pentru activitatea optima.
Semnalele pro-apoptotice ale legarii CD95 (agentii antineoplazici supraregleaza receptorul sau induc expresia ligantului) sau eliberarea citocromului c activeaza initiatorul caspazelor (caspaza-8 si caspaza-9), care ulterior activeaza caspazele efectoare (caspazele-3, -6 si -7) care desavarsesc liza celulara.
Stresul oxidativ poate induce apoptoza determinand leziuni ale componentelor celulare (ex.ADN) si unele studii sustin ca ROS sunt mediatorii din aval ai apoptozei(Johnson). Totusi, exista numeroase do ca apoptoza nu necesita ROS si ca generarea lor este un eveniment tardiv, dupa ce celula deja este intrata in ciclul mortii celulare programate(Clutton, Schandra). Dovada acestui lucru este ca generarea ROS in mitocondrie apare numaidupace apoptoza este initiatade eliberarea de citocrom c.
In contrast cu apoptoza indusa de stresul oxidativ, stresul oxidativ excesiv inhiba activitatea caspazelor(367, 369) si apoptoza drog-indusa, in acest fel interferand cu abilitatea agentilor antineoplazici de a distruge celulele tumorale (354, 357). Aldehidele electrofile, cum este tetrapeptid-aldehida( acetil-Tir-Val-Ala-Asp-H) care a fost folosita pentru a caracteriza caspaza-l, se leaga covalent de gruparea sulfhidril a restului de cisteina la nivelul situsului activ al caspazei si ii inhiba activitatea.(374). Astfel, generarea aldehidelor,avand ca rezultat inhibarea caspazelor,pot fi cauza scaderii eficacitatii agentilor antineoplazici in cazul stresului oxidativ excesiv. Daca este asa, antioxidantii pot creste activitatea antineoplazica a chimioterapicelor prin scaderea generarii de aldehide in cazul unui stres oxidativ exagerat drog-indus.
Generarea aldehidelor prin peroxidare lipidica in timpul stresului oxidativ indus de chimioterapie poate interfera direct si cu calea receptorului CD95 al apoptozei drog-induse. Receptorul CD95 al mortii are un domeniu extracelular bogat in cisteina care il face o tinta pentru agentii electrofili cum sunt aldehidele. Aceste legaturi inter aldehide si receptorul mortii pot mima efectul anticorpilor antireceptor CD95,interferand cu apoptoza drog-indusa.De aceea, antioxidantii, prin scaderea nivelului aldehidelor, pot facilita apoptoza drog-indusa via calea receptorului CD95.
Concluzii
Stresul oxidativ interfera cu multe functii celulare, cum sunt progresia ciclului celular si caile apoptozei, si poate micsora abilitatea agentilor antineoplazici de a distruge celulele. Efectul este mediat,cel mai adesea, prin multele aldehide rezultate din peroxidarea lipidica indusa de stres. Deoarece multe chimioterapice folosite in terapia cancerului determina stres oxidativ dovedit, scazand acest stres prin administrarea de antioxidanti se poate creste eficienta tratamentului. Totusi, crescand citotoxicitatea agentilor antineoplazici,vor fi afectate atat celulele tumorale,cat si cele normale. Astfel, desi anumiti antioxidanti par sa previna dezvoltarea unor efecte secundare induse de anumite chimioterapice ( coenzima Q10 pentru cardiotoxicitatea antraciclinelor si glutationul pentru nefrotoxicitatea cisplatinului), efectele secundare rezultate din toxicitatea asupra tesuturilor cu proliferare rapida,cum sunt mielosupresia, pierderea parului si mucozita, pot fi exacerbate de antioxidanti.
Cu siguranta sunt necesare studii mai profunde pentru a clarifica impactul stresului oxidativ si antioxidantilor asupra activitatii antineoplazice si a efectelor secundare ale multitudinii de droguri si combinatii de droguri existente in utilizarea clinica.
O problema majora in Romania este poluarea atmosferei provocata de degajarea in aer a gazelor si particulelor fine (cenusii) prin furnale, turnurile s [...] |
Asa cum sugereaza si denumirea, radicalii liberi sunt structuri moleculare instabile, reactive, ce se nasc in organism in orice moment - la nivel [...] |
Radiatiile ionizante (prin produsii toxici rezultati si din radioliza apei), pot produce, in plus, direct sau indirect, leziuni ale moleculelor d [...] |
Copyright © 2010 - 2026
: eSanatos.com - Reproducerea, chiar si partiala, a materialelor de pe acest site este interzisa!
Informatiile medicale au scop informativ si educational. Ele nu pot inlocui consultul medicului si nici diagnosticul stabilit in urma investigatiilor si analizelor medicale la un medic specialist.
Termeni si conditii - Confidentialitatea datelor - Contact
Despre cancerul |
| Alte sectiuni |
|
Ai o problema medicala? |